Aminosäuren und Proteine
- Opsin ist ein Protein/Eiweiß.
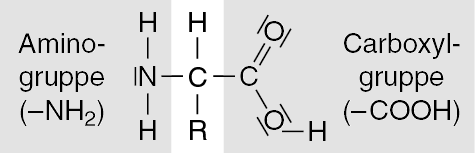
- Allgemeine Formel:

Die Carboxylgruppe einer Aminosäure reagiert mitder Aminogruppe einer zweiten Aminosäure unterWasserabspaltung. Die entstehende Bindung isteine Peptidbindung.
- Die Primärstruktur gibt die Reihenfolge derAminosäurereste im Protein an. Da die Reihenfolge der Aminosäuren Konsequenzen für dieSekundär- und Tertiärstruktur hat, bestimmt diePrimärstruktur auch die räumliche Struktur desProteins und damit auch dessen Funktionen.
- Es sind Wasserstoffbrückenbindungen, welchedie spiralig gewundene Struktur stabilisieren.Ein schraubig gewundener Abschnitt einesProteins wird als a-Helix (Alpha-Helix) bezeichnet.
Wissensteil:
Proteine, umgangssprachlich auch Eiweiße genannt, sind Makromoleküle, die aus den Ele
menten Kohlenstoff, Wasserstoff, Sauerstoff, Stickstoff und Schwefel aufgebaut sind. Proteine verleihen der Zelle nicht nur Struktur, sie sind auch die molekularen „Maschinen“, die Reaktionen katalysieren, Stoffe transportieren, Ionen pumpen und Signalstoffe erkennen.
„Betrachtet man die DNA als den Bauplan des Lebens, so sind die Proteine Ziegel und Mörtel. Doch damit nicht genug, sie stellen auch das nötige Werkzeug für den Zusammenbau einer Zelle oder eines Organismus und übernehmen sogar die Rolle der Handwerker, die den Aufbau durchführen. Unsere Gene liefern zwar die Vorlagen, aber was wir sind, sind wir durch unsere Proteine.“(Russel F. Doolittle)
Das Wort Protein wurde 1838 von Jens Jakob Berzelius von dem griechischen Wort proteuo („ich nehme den ersten Platz ein“, von protos, „erstes“, „wichtigstes“) abgeleitet. Es betont die Bedeutung der Proteine für die Lebewesen.
Bausteine der Proteine sind die Aminosäuren, die durch Peptidbindungen zu Ketten verbunden sind. Beim Menschen handelt es sich um 21 verschiedene Aminosäuren. Aminosäureketten mit einer Länge von zwei bis 100 Aminosäuren werden als Peptide bezeichnet, erst bei einer Aminosäurenanzahl von mehr als 100 spricht man von Proteinen.
Das Rückgrat der Proteine entsteht durch eine Verbindung der Aminogruppe einer Aminosäure mit der Carboxylgruppe (Säuregruppe) der nächsten Aminosäure. Dabei wird ein Wassermolekül frei. Die Bindung CO-NH ist eine Peptidbindung, die entstehende Verbindung ist ein Peptid. Kurze Peptide nennt man Oligopeptide, längere Moleküle bezeichnet man als Polypeptide. Jedes Peptid trägt an einem Ende, dem N-Terminus, eine freie Aminogruppe, und am anderen Ende der Kette, dem C-Terminus, eine freie Carboxylgruppe (Säuregruppe).
Proteine liegen in der Zelle nicht als Fäden vor. Sie können sich zu mannigfaltigen Formen falten und bilden komplizierte dreidimensionale Strukturen. Im einfachsten Fall bildet das Polypeptid nur eine Sekundärstruktur wie α-Helix oder β-Faltblatt aus. In der Regel werden diese Sekundärstrukturen aber nur von kurzen Bereichen der Polypeptidkette ausgebildet, zwischen denen Loop-Strukturen oder relativ ungeordnete Bereiche liegen.
Jedes Protein hat eine unverwechselbare Oberflächenstruktur. Während Faserproteine eine langgestreckte Gestalt annehmen, sind globuläre Proteine etwa kugelförmig. Die räumliche Anordnung der Proteine wird durch die Seitenketten ihrer Aminosäurereste beeinflusst. Manche dieser Seitenketten ziehen sich an – z.B. zwei unterschiedlich geladene Gruppen – andere stoßen sich ab – z.B. zwei gleich geladene Gruppen. Daher falten sich die meisten Polypeptidketten so, dass die polaren Reste an der Oberfläche, die unpolaren im Inneren des Moleküls zu liegen kommen.
Die Mannigfaltigkeit der Formen spiegelt sich in vielfältigen Funktionen wieder. In ihren Funktionen unterschieden sich die Proteine grundsätzlich. Jedes Protein erfüllt eine ganz bestimmte Aufgabe: Es ist Baustein einer Membran und grenzt damit ein Kompartiment der Zelle ab oder es ist Enzym und katalysiert eine ganz bestimmte chemische Reaktion, oder es ist Teil einer Aktinfibrille und trägt dazu bei, dass sich Lebewesen bewegen können.
Opsin ist ein Transmembranprotein. Zusammen mit Retinal bildet Opsin das lichtempfindliche Pigment-Molekül Rhodopsin, das durch einen Reiz aktiviert werden kann und den Beginn der Signaltransduktion in den Stäbchen des Auges bildet. Das Opsin ist der Bestandteil der Sehpigments, der entscheidet, in welchem Bereich des Lichtspektrums der Sehfarbstoff besonders gut absorbiert.
.
!

