Wissensteil:
Salze sind im festen Zustand kristalline Verbindungen, die aus Ionen aufgebaut sind. Beim Lösen in Wasser können die Kationen und Anionen der Salze mit dem Ampholyten Wasser als Brönstedsäuren oder -basen reagieren.
Kationen als Säuren
Kationen, die die korrespondierenden Säuren schwacher Basen sind, können als Brönstedsäuren reagieren. Einige Metallionen wie Al3+(aq)- und Fe3+(aq)-Ionen bilden auch saure Lösungen.
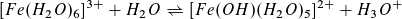
Der Säurecharakter beruht darauf, dass Wassermoleküle, die die nächsten Nachbarn sind, durch das mehrfach positiv geladene Metallion so stark polarisiert werden, dass es zur Abspaltung eines Protons kommen kann. Lösungen von hydratisierten Metallionen sind umso stärker sauer, je höher die Ladung und je kleiner der Radius, d. h. je größer die Ladungsdichte des Ions ist. Hydratisierte Alkali- und Erdalkalimetallionen haben aufgrund ihrer geringen Ladungsdichte eine so geringe Säurestärke, dass man das Ausmaß der Säure-Base-Reaktion mit Wasser als vernachlässigbar ansehen kann.
Anionen als Basen
Anionen, die korrespondierende Basen schwacher Säuren sind, reagieren gegenüber Wasser als Brönstedbasen. Sie bilden alkalische Lösungen. Die Anionen sehr starker bzw. starker Säuren sind sehr schwache bzw. schwache Basen, sie gehen deshalb keine Säure-Base-Reaktionen mit den Wassermolekülen ein.
Neutrale Salzlösungen
Die wässrige Lösung eines Salzes ist nur dann neutral, wenn weder die Kationen noch die Anionen mit Wassermolekülen in merklichem Ausmaß reagieren (z. B. Na+Cl -) oder wenn die Säurestärke der einen Ionenart gleich der Basestärke der anderen ist (z. B. CH3COO -NH4+).

